Сегодня мы поговорим о том, каким образом
прибор «Биомедис Тринити» оказывает влияние на внутриклеточные процессы, т.е. на самые «корневые» процессы
происходящие в организме на физическом плане. Ведь клетка это - наименьшая единица жизни, несущая гены и способная к обмену
веществ, самопочинке и воспроизведению и от того с какой эффективностью функционирует клетка зависит состояние всего
организма. Здоровье организма – это здоровье каждой
клетки. Вне клетки жизни нет. Мы реально увидим
как прибор «Биомедис-Тринити» влияет на активность единичной клетки.
1.
Строение клетки
Для полного понимания рассмотрим как устроена клетка. Клетки всех организмов сходны по строению и химическому
составу и такого поверхностного обзора в нашем случае будет достаточно. И так:
Рис.1 Строение клетки
Плазматическая мембрана (плазмалемма)
В основе всех мембран клетки лежит двойной слой молекул липидов.
Рис.2 Строение мембраны
Их гидрофобные (боящиеся воды) «хвосты», состоящие из остатков молекул жирных
кислот, обращены внутрь двойного слоя. Снаружи располагаются гидрофильные (любящую
воду) «головки», состоящие из остатка молекулы спирта глицерина. В состав
мембран чаще всего входят фосфолипиды и гликолипиды (их молекулы наиболее
полярны), а также жиры и жироподобные вещества (например, холестерин). Липиды
являются основой мембраны, обеспечивают ее устойчивость и прочность, т.е.
выполняют структурную (строительную) функцию. Эта функция возможна благодаря
гидрофобности липидов. К заряженным головкам липидов, с помощью
электростатических взаимодействий прикрепляются белки. Мембранные
белки выполняют структурные, каталитические и транспортные функции. В
зависимости от расположения различают погруженные, периферические и
пронизывающие белки. Погруженные белки слегка погружены в двойной слой липидов
и являются ферментами, которые катализируют различные биохимические реакции.
Периферические белки расположены на поверхности двойного слоя липидов. Они
стабилизируют расположение погруженных белков-ферментов. Пронизывающие белки
пронизывают мембрану насквозь и выполняют транспортные функции. На наружной
поверхности мембраны расположены молекулы углеводов (олигосахариды),
которые выполняют рецепторные функции. Олигосахариды воспринимают факторы
внешней среды клетки и обеспечивают ее реакцию, изменяют проницаемость
мембраны, обеспечивают «распознавание» клеток одного типа и соединение их в
ткани. Совокупность олигосахаридов на поверхности животной клетки называется
гликокаликсом.
Функции плазматической мембраны
1.
Барьерная функция. Мембрана ограничивает проникновение в клетку чужеродных,
токсичных веществ.
2.
Регуляторная. Олигосахариды, располагающиеся на поверхности плазматической
мембраны выполняют роль рецепторов, воспринимающих действие различных веществ и
изменяющих проницаемость мембраны.
3.
Каталитическая. На поверхности мембран располагаются многочисленные
ферменты, катализирующие биохимические реакции.
4.
Мембранный транспорт. Различают несколько видов мембранного транспорта.
Цитоплазма
Цитоплазма представляет собой внутреннее содержимое клетки и состоит из
основного вещества (гиалоплазмы), органоидов и включений.
Гиалоплазма - жидкая (желеобразная) часть клетки, представляет собой раствор
органических и неорганических веществ.
Ядро - важнейшая составная часть эукариотической клетки. Ядро не является
органоидом клетки, так как во время деления клетки распадается.
Рис. 3 Строение ядра
Функции ядра:
1.
хранение генетической информации и ее воспроизводство
2.
управление жизнедеятельностью клетки путем реализации генетической
информации, заключенной в ДНК.
В строении ядра различают 4 основных компонента:
- ядерная
оболочка (кариолемма)
- ядерный
сок (кариоплазма, кариолимфа, нуклеплазма)
- ядрышко
- хроматин.
Оформленное ядро присутствует в клетке только в периоде между ее делениями
(в интерфазе). Во время деления клетки оболочка ядра распадается, исчезает
ядрышко, а хроматин спирализуется и преобразуется в хромосомы.
Ядерная оболочка состоит из 2 близко расположенных мембран - наружной и
внутренней. Между ними находится пространство. Наружная мембрана переходит в
мембрану эндоплазматической сети, к ней могут быть прикреплены рибосомы. Через
определенное расстояние обе мембраны сливаются друг с другом, образуя отверстия
- ядерные поры. Число пор может изменяться в зависимости от активности ядра.
Функции ядерной оболочки:
1.
Защитная. Защищает генетический материал от различных отрицательных
воздействий.
2.
Обеспечивает локализацию (размещение) генетического материала в определенном
месте клетки.
3.
Через поры ядра происходит обмен веществами между ядром и цитоплазмой. В
ядро поступают белки-гистоны и рибосомные белки, синтезирующиеся в цитоплазме.
Из ядра в цитоплазму перемещаются и-РНК, т-РНК, субъединицы рибосом.
4.
Ядерная оболочка обеспечивает определенную реакцию среды внутри ядра, что
необходимо для его нормального функционирования
5.
Структурная. Ядерная оболочка придает ядру определенную форму
В контексте данной статьи мы не
будем рассматривать строение и функции остальных составляющих клетки. Подводя итог вышесказанного можно сказать (в
сильно упрощенной модели), что клетка – это многослойная, упругая, пористая сфера
заполненная жидкостью. В клетку и из клетки через поры входят и выходят
(транспортируются) определенные вещества. Т.е. активность клетки зависит прежде
всего от правильного функционирования
мембран.
2. Акустоэлектрические колебания клеточных
мембран.
Давайте рассмотрим модель клетки,
так будет проще для понимания. Клетку можно сравнить с резиновым пористым шариком
наполненным жидкостью, внутри которой еще один резиновый, пористый шарик (по
принципу матрешки) тоже заполненный жидкостью. Наверное, каждый из Вас когда
либо заполнял водой резиновый шарик и
бросал его с окна или балкона. Помните как этот шарик «играл» в руках? У этого
шарика есть собственная частота колебаний или если назвать по другому –
резонансная частота. Т.е. если этот шарик подвесить и ударить по нему, то можно
наблюдать периодическое изменения геометрии шарика. Колебания могут быть
продольными или поперечными. В свою очередь продольные и поперечные колебания
могут быть симметричными и несимметричными [1].
Рис.4 Различные виды колебаний
мемебраны.
Частота колебаний зависит от размеров
шарика, от модуля упругости резины, от массы воды заполняющий шарик, от массы
самого шарика и от других параметров. Живая
клетка в ходе жизнедеятельности подобно резиновому шарику тоже находится в
постоянном колебательном движении (имеется ввиду колебания плазматической
и ядерной мембраны). Такие колебания
называются акустическими. А поскольку мембраны поляризованы, то
возбуждение акустических колебаний связано с одновременным возбуждением
электрических колебаний, длина волны которых совпадает с акустическими - то
есть с возбуждением в мембранах акустоэлектрических
колебаний и волн.
В клетках, электрически симметричных и
нормально функционирующих, не имеется никаких условий для преобладания
некоторых резонансных частот [2],[3],[4]. Именно поэтому обмен энергии между
всеми элементами клетки, включая молекулы белка, дает как результат появление
шумовых колебаний со спектром частот, фактически не отличимым от спектра
частот, излучаемого мертвыми органами при температуре, равной температуре
живого организма. Распределение энергии между различными частотами колебаний
соответствует распределению, определенному формулой Планка. Различные
отклонения от нормального функционирования клетки всегда сопровождается
появлением электрической асимметрии. Электрическая асимметрия, в свою очередь,
вызывает преобладающее возбуждение колебаний или некоторых определенных
частот, или в некоторых определенных (иногда довольно узких) частотных полосах.
В результате амплитуды акустоэлектрических волн, соответствующих этим частотам,
в клеточных мембранах увеличиваются. С другой стороны, имеются более чем 1000
различных типов молекул белка в клетках, чьи резонансные полосы накладываются
на полосу акустоэлектрических колебаний. Дипольные колебания молекул белка
поддерживаются за счет метаболизма. Поле стоячих акустоэлектрических волн,
имеющих резонансные частоты в мембранах, наиболее эффективно взаимодействует с
теми дипольными колебаниями молекулы белка, которые имеют те же резонансные
частоты, что и колебания мембраны. Энергия колебаний диполей молекул белка,
приближающихся к мембране и прилипающих к ней, передастся субструктуре и
приводит к возбуждению акустоэлектрических колебаний и волн. Существенно,
чтобы субструктура конгломератов белка функционировала как единая система.
Молекулы белка в этом случае взаимно синхронизируются так, что амплитуда
колебаний резко увеличивается, обеспечивая самовозбуждение когерентных
акустоэлектрических колебаний и волн. Устойчивое состояние нормально
функционирующих клеток, как уже было сказано, это состояние, характеризуемое
электрической симметрией. Его нарушение приводит к возбуждению
акустоэлектрических волн и связанных с ними сил. Вот почему возбуждение
акустоэлектрических волн сопровождается появлением сил, восстанавливающих
электрическую симметрию. Другими словами, акустоэлектрические волны являются
инструментом, с помощью которого клетки (и многоклеточные организмы)
поддерживают и восстанавливают клеточный гомеостаз.
Однако
для проведения быстрого и эффективного строительства субструктур белка
электрическая компонента поля должна иметь большую амплитуду. Обычно первое
строительство субструктур белка имеет место в системе со слабо отмеченными
резонансными свойствами, определенными беспорядками, часто не яркими,
электрической симметрии. Поскольку большее количество новых молекул белка
тянется к субструктурам, энергия, переданная ими, увеличивает поле. Это
приводит к лучшему формированию конгломератов белка на мембранах и укреплению
резонансных свойств системы. В результате шумовые колебания постепенно
преобразовываются в когерентные колебания.
Восстановление
нормального функционирования и электрической симметрии клеток приводит к
завершению действия сил, возбуждающих акустоэлектрические волны. В результате
временные субструктуры белка, появляющиеся на
клеточных
мембранах при нарушениях функционирования, постепенно отделяются после
нормализации функций.
Выше, появление акустоэлектрических волн в клетках
было описано для случаев, когда восстановление нормального функционирования
организм проводил самостоятельно, без воздействия внешнего поля. Однако в угнетенных
клетках многоклеточных организмов такое восстановление может проходить медленно
или совсем не иметь место. В этих случаях внешние
поля могут быть использованы для ускорения восстановительных процессов.
3. Как вызвать акустоэлектрические
колебания клеточных мембран внешними полями?
Влияние
электромагнитного излучения низкой интенсивности СВЧ диапазона (от 30 до 300
ГГц) на функционирование живых организмов было установлено еще в середине 60-х
годов, это была ранняя стадия изучения этих колебаний в живых организмах. Позже
была установлена возможность острорезонансного характера отклика живых
организмов на КВЧ излучение [2]. Также было обнаружено, что КВЧ излучение
вызывает колебания в клеточных мембранах. В этом случае, характер отклика
биологической клетки на воздействие КВЧ меняется с частотой излучения и
представляет собой ряд максимумов [3]. Были разработаны и созданы ряд
терапевтических аппаратов использующих КВЧ волны, которыми пользуются до сих
пор. Однако со временем возникший бум вокруг КВЧ терапии постепенно затих в
силу небольшой эффективности и на сегодняшний день применение данного вида
терапии сводится к рефлексотерапии, где в качестве воздействующего фактора
используется КВЧ излучение. Но в ходе проведенных нами исследований по
радиолокационному зондированию биообъектов в СВЧ и КВЧ диапазоне с целью
получения электромагнитных профилей (набор статистической информации для
создания диагностической базы) обнаружился интересный факт. Мы пришли к тому,
что длительное зондирование биообъекта малыми дозами СВЧ и КВЧ излучения со
сложной структурой приводило к исчезновению информационных признаков патологий
в электромагнитных профилях. Выяснилось, что причиной является именно
использование многочастотного, сложно модулированного
излучения с обратной связью с биообъектом. Теоретические расчеты показывают,
что резонансные частоты продольных симметричных акустических колебаний мембран
клеток упоминавшиеся во 2-й главе имеют порядок сотен МГц [1], а резонансные
частоты поперечных несимметричных колебаний имеют порядок десятков МГц (именно
эти виды колебаний являются самыми
эффективными для интенсификации обменных процессов в объеме клетки) [1]. Т.е.
падающие СВЧ и КВЧ волны должны были вызвать низкочастотные колебания,
отличающиеся по частоте от падающей в 1000 и в 10000 раз. И эта проблема у нас
уже была решена само по себе применением многочастотной
синхронизации. Говоря проще, при воздействии на поверхность мембраны клеток
двух и более гармонических сигналов с такими близкими частотами, чтобы их
разность была равна
частоте акустических колебаний, возникает резонанс [13]. При этом энергия электромагнитного поля с максимальной эффективностью преобразуется в энергию механических колебаний мембраны клетки. Далее мы поговорим о том, каким образом можно удостовериться в справедливости вышесказанного. Опыт подтверждает теорию! И так, нам нужен простой способ. Удобным и дающим ценную информацию о состоянии клеточной поверхности является метод микроэлектрофореза.
частоте акустических колебаний, возникает резонанс [13]. При этом энергия электромагнитного поля с максимальной эффективностью преобразуется в энергию механических колебаний мембраны клетки. Далее мы поговорим о том, каким образом можно удостовериться в справедливости вышесказанного. Опыт подтверждает теорию! И так, нам нужен простой способ. Удобным и дающим ценную информацию о состоянии клеточной поверхности является метод микроэлектрофореза.
4. Электроотрицательность клеточных ядер
(ЭОЯ).
Известно, что
большинство клеток животного
происхождения эритроциты, лейкоциты, тромбоциты и др. и микробные клетки на
своей поверхности несут определенный заряд. Этот заряд определяет
электрокинетические свойства клеток, то есть скорость их передвижения в
электрическом поле, которая определяется методом микроэлектрофореза . Обычно поверхность живых
клеток имеет отрицательный заряд, величина которого зависит от количества
адсорбированных на их поверхности молекул или ионов. Как известно, клеточные мембраны различных типов, в
зависимости от того, частью каких органелл они являются (плазматическая
мембрана, мембрана, окружающая
митохондрии, эндоплазматический ретикулум и др.), отличаются по своей структуре и химическому составу. Функционально
можно выделить две категории плазматических мембран. Одна категория связана с
проникновением различных веществ в клетку и из нее, другая выполняет ферментативные функции.
Эти свойства клеточных мембран определяют электрофоретическую
подвижность клеточных ядер или электроотрицательность
клеточных ядер [5]. Что такое электрофоретическая подвижность клеточных ядер? Передвижение клеток, также как и других
заряженных частиц, в электрическом поле происходит в результате образования
разности потенциалов между дисперсной фазой и дисперсионной средой. Такой
потенциал называется электрокинетическим. Возникновение потенциала на границе
двух фаз всегда связано с возникновением
на поверхности раздела электрического заряда. Причиной возникновения заряда на
поверхности клеток может быть или адсорбция ионов из растворов или локализация
диссоциирующих групп дисперсной фазы состоящей из слоя адсорбированных на поверхности ионов и из слоя противоположно
зараженных ионов, которые сорбируются на первом слое. Это двойной электрический
слой, точнее ионная атмосфера, образующая диффузионный слой, строение которого
зависит от концентрации ионов в среде. Таким образом, можно сказать, что
образование заряда на поверхности
раздела двух фаз обусловлено ассиметричным
распределением ионов. Биологические свойства
клеточных ядер играют не меньшую роль в жизнедеятельности клетки, чем
биоэлектрические свойства клеточной оболочки. Было установлено, что увеличение
плотности заряда на поверхности ядра соответствует периоду репликации ДНК и,
как следствие, увеличению активного метаболизма, связанного с синтезом РНК и белков. Это отражается на свойствах
поверхности клеточной цитоплазматической мембраны, поскольку существует связь
между цитоплазматической мембраной клетки и плазматической мембраной, окружающей
ядро. Исследования подтверждают взаимосвязь между интенсивными метаболическими
процессами (репликация ДНК) и свойствами ядерных мембран и, как результат, электрофоретической
подвижностью ядер [5]. Наблюдая
за движением отдельных клеток или частиц под микроскопом можно измерять
электрокинетический потенциал частиц и клеток любого размера. Это достигается
наложением электрического поля
на взвесь клеток.
Рис.5
Установка для исследования ЭОЯ клетки.
Клетки при этом начинают двигаться в
зависимости от знака их заряда. Так
мембрана клетки более электороотрицательна относительно межклеточной жидкости,
цитоплазма клетки – относительно мембраны, ядро клетки – относительно
цитоплазмы. Если их поместить в
переменное электрическое поле, то этот биологический закон можно наблюдать под
микроскопом – как будто все они «танцуют вальс» друг относительно друга. Это
впервые открыл профессор В.Г.Шахбазов в 80-х годах прошлого столетия . Но не
только открыл, но и достоверно установил, что если ядро клетки не «танцует», то
клетка не выполняет своих биологических функций, и, что еще более поразительно,
количество «танцующих» ядер строго соответствует биологическому возрасту
человека. Подтвердив все вышесказанное огромным экспериментальным материалом,
В.Г.Шахбазов в 1986 году запатентовал метод, назвав его «Способ определения
биологического возраста человека» [6]. Этот способ по настоящее время является
наиболее достоверным методом определения по сути изношенности организма. Исследованиями В.Г. Шахбазова с
сотр. установлено, что электрический заряд ядер имеет важное значение в
реакции клетки и всего организма на действия разных факторов, как экзогенных,
так и эндогенных (в том числе и внешних электромагнитных полей) [9]. Величина заряда ядра коррелирует с уровнем
функциональной активности клетки и организма. Показатели
электроотрицательности ядер отражают изменения в ядре баланса различно заряженных молекул, а также
электрической поляризуемости ядра и внутриядерных структур. Поскольку электрический потенциал оболочки ядра играет важную роль в
транспорте веществ между ядром и цитоплазмой,
поддержание его на определенном уровне необходимо для нормального функционирования клеток. Установлена тесная прямая зависимость электрокинетических
свойств ядер от возраста человека. С возрастом заряд ядра постепенно снижается.
Многолетними работами автора установлено, что биоэлектрические свойства
нативных клеточных ядер, в том числе электрокинетический потенциал, характеризует потенциальную
энергию генома (ПЭГ). ПЭГ - это те
энергетические свойства ядерного генома, от которых зависит развитие разных
проявлений количественной наследственности, в частности неспецифической
устойчивости. Параметр ЭОЯ является
чувствительным маркером, позволяющим оценивать динамику течения болезни на
разных стадиях развития патологии и фиксировать эффективность лечения при различных заболеваниях.
5. Практические результаты.
Известно, что
буккальные эпителиоциты (или по-простому – клетки из внутренней поверхности
щеки), как и все эпителиальные клетки слизистых оболочек, играют важную роль
в системе гуморально - клеточного гомеостаза. В последние годы внимание исследователей
в качестве материала для неинвазивной диагностики привлекает буккальный
эпителий (БЭ).

Рис.6 Клетки буккального
эпителия под микроскопом с увеличением 200Х
Рис.7
Клетки буккального эпителия под микроскопом с увеличением 400Х
Взятие материала с внутренней поверхности щеки –
неинвазивная процедура. БЭ можно рассматривать как пограничную
зону между
внешней и внутренней средой организма. Таким образом, изменения функциональной
активности клеток БЭ (процессы клеточного обновления и дифференцировки,
экспрессия различных сигнальных молекул) во многом отражают состояние
локального и системного гомеостаза организма или его нарушения при
патологических состояниях. Следовательно, БЭ, доступный для прижизненного
гистологического исследования, может служить источником
важной диагностической
и прогностической информации о состоянии здоровья, стрессовых
воздействиях, влиянии факторов внешней среды, соматической патологии и
биологического возраста человека [7],[8],[9],[10],[11],[12]. Исходя из всего
вышесказанного мы провели исследование по выявлению влияния сложно модулированного,
многочастотного электромагнитного излучения прибора Биомедис «Тринити» на
электроотрицательность клеточных ядер буккального эпителия. Мы специально
провели опыты методом in vitro (в стекле), чтобы доказать влияние
данного вида излучения именно на внутриклеточные процессы, исключая влияние
других внеклеточных механизмов регуляции метаболизма в живом организме. Ниже
приводятся результаты данного исследования.
Рис.8 Внешний вид установки для
наблюдения за ЭОЯ клеток.
Материалы и методы: Опыты
проводились методом in vitro. Объектом исследования служили клетки буккального эпителия, взятые у
доноров из полости рта. Донорами служили мужчины в возрасте 32 (опыт А) и 50
(опыт В) лет. Клетки помещали в раствор следующего состава: Среда Игла МЕМ с
солями Хэнкса, глутамин. Клетки
наносились на предметное стекло модифицированной камеры Горяева, которая вместе
с приклеенными электродами являлась электрофоретической камерой. Камера сверху
накрывалась покровным стеклом. Температура камеры поддерживалась в районе 36
градусов Цельсия с помощью резистивного термостата с микропроцессорным
управлением. Материал электродов – платина. Сигнал на электроды подавался с
генератора сигналов специальной формы АКИП 3407/4А. Амплитуда сигнала между электродами – 10 В. Средняя
сила тока через электрофоретическую камеру – 140 мкА. Форма сигнала –
биполярная, синусоидальная. Частота сигнала на электродах электрофоретической
камеры в опыте А – 1.6 Гц, в опыте В – 0.6 Гц. Наблюдение велось через
микроскоп Levenhuk D870T с увеличением в 400
Х, с вводом изображения в ПК через цифровую видеокамеру разрешением 8 Мп. Критерием
действия облучения служила электрофоретическая подвижность ядер клеток, которая
учитывает электроотрицательность ядра, по величине смещения в переменном электрическом поле.
Подсчет величины смещения ядра клетки проводился автоматически, с помощью
программного обеспечения «Tracker 5.0.2» до начала облучения и после 35
минутного облучения прибором Биомедис «Тринити». Программа используемая на
приборе – «Активация жизненной энергии». Режим работы – 4.
Результаты:
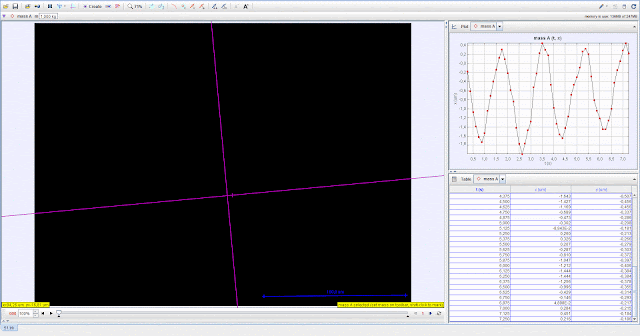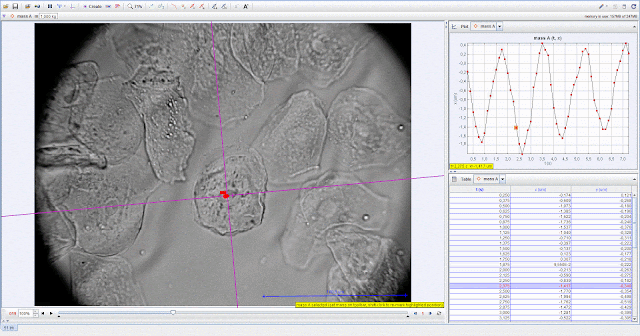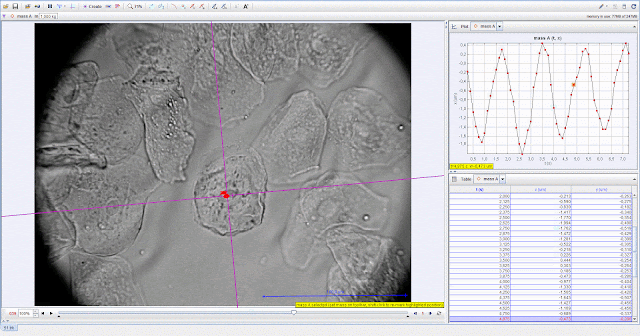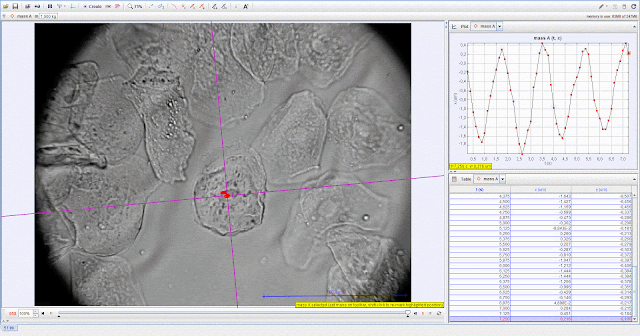
Рис.9
Подвижность ядра клетки в переменном электрическом поле до воздействия прибора
Биомедис «Тринити». Опыт А.
Рис.10
Подвижность ядра клетки в переменном электрическом поле после 35 минутного
воздействия прибора Биомедис «Тринити». Опыт А.
На рисунках 9 и 10
отображены результаты обработки видеофайлов записанных до и после воздействия
прибором Биомедис «Тринити» в опыте А.
Рис.11
Сравнение подвижности ядра клетки в переменном
электрическом поле до и после 35 минутного воздействия прибора Биомедис
«Тринити». Опыт А. Красный график – «до», зеленый график – «после».
На рисунке 11 отображен
график, где проводится сравнение полученных результатов в опыте А. Из графика
видно, что средняя амплитуда смещения ядра клетки до воздействия составляет 0.8
мкм. После воздействия амплитуда смещения увеличилось на 125% и составила 1.8
мкм.
Рис.12
Подвижность ядра клетки в переменном электрическом поле до воздействия прибора
Биомедис «Тринити». Опыт В.
Рис.13
Подвижность ядра клетки в переменном электрическом поле после 35 минутного
воздействия прибора Биомедис «Тринити». Опыт В.
На рисунках 12 и 13
отображены результаты обработки видеофайлов записанных до и после воздействия
прибором Биомедис «Тринити» в опыте В.
Рис.14
Сравнение подвижности ядра клетки в переменном
электрическом поле до и после 35 минутного воздействия прибора Биомедис
«Тринити». Опыт В. Зеленый график – «до», красный график – «после».
На рисунке 14 отображен
график, где проводится сравнение полученных результатов в опыте В. Из графика
видно, что средняя амплитуда смещения ядра клетки до воздействия составляет 2
мкм. После воздействия амплитуда смещения увеличилось на 60% и составила 3.2
мкм.
Выводы:
Полученные результаты свидетельствуют об увеличении величины
электроотрицательности ядер клеток буккального эпителия под влиянием облучения,
что говорит о ярко выраженном стимулирующем действии излучения прибора Биомедис
«Тринити» на внутриклеточные процессы. Следует отметить, что эффективность
увеличения величины электроотрицательности ядер зависит от исходного состояния
донора.
Литература:
1. Харланов А.В. Акустоэлектрические колебания клетки. Диссертация на соискание ученой степени кандидата
физико-математических наук. 2006 г.
2. Бецкий О. В., Лебедева Н. Н. Современные представления о механизмах воздействия низкоинтенсивных миллиметровых волн на биологические
объекты. Миллиметровые волны в биологии и медицине. 2001. № 3(24). С.
5–19.
3. Czapla Z., Cieślik J. Electrophoretic Mobility of Cell Nuclei (EMN) index –relation to biological and physical properties of the cell. Anthropological Review. 1998. Vol. 61. Р. 93–101.
4. Девятков Н. Д., Голант М. Б., Бецкий О. В. Миллиметровые волны и их роль в процессах жизнедеятельности. Москва: Радио и связь, 1991. 168 с.
5. Шкорбатов Ю. Г., Шахбазов В. Г. Биоэлектрические свойства клеточных ядер. Успехи совр. биол. 1992. Т. 112,
вып. 4. С. 499–510.
6. Способ исследования функционального состояния человека: пат. 2009494, Россия. C1 RU GO1 №33/483 / В. Г. Шахбазов, Ю. Г. Шкорбатов. Открытия. Изобретения. 1994. № 5.
7. Shckorbatov Y. G., Shakhbazov V. G., Navrotskaya V. V., Grabina V. A., Sirenko S. P., Fisun A. I., Gorobets N. N.,
Kiyko, V. I. Application of intracellular microelectrophoresis to analysis of the influence of the low-level microwave radiation on electrokinetic properties of nuclei in human epithelial cells. Electrophoresis. 2002. Vol. 23, N 13. Р. 2074–2079.
8. Сиренко С. П., Григорьева Н. Н., Шахбазов В. Г., Фисун А. И., Белоус О. И., Горобец Н. Н., Кийко В. И. Действие сантиметровых и миллиметровых электромагнитных волн линейной и круговой поляризации на клетки буккального эпителия человека. Материалы XI Междунар. Крымской конф. «СВЧ-техника и телекомуникационные технологии» (КрыМиКо’2001). 2001. С. 97–98.
9. Белоус О. И., Брюзгинова Н. В., Сиренко С. П., Фисун А. И. Контроль биологической эффективности действие электромагнитных полей миллиметрового диапазона. Радиофизика и электроника. 2015. Т. 6(20), № 4. С 98–102.
10. Шахбазов В. Г., Колупаева Т. В., Григорова И. А., Возницина К. Б. Изменение биологического возраста у больных с энцефалопатиями. Тезисы доклада, представленного на III Конгрессе геронтологов и гериатров Украины. 2000.
11. Мячина О. В., Зуйкова А. А., Пашков А. Н. Электрокинетическая активность клеток буккального эпителия у больных гипертонической болезнью. Сибирский медицинский журнал. 2012. Т. 27, № 2. C. 120–122.
12. Arkhypova K. A., Bilous O. I., Bryuzginova N. V., Fisun A. I., Malakhov V. O., Nosatov A. V., Sirenko S. P., Yemets B. G.
Role of mikrowave radiation in self-blood therapy.
3. Czapla Z., Cieślik J. Electrophoretic Mobility of Cell Nuclei (EMN) index –relation to biological and physical properties of the cell. Anthropological Review. 1998. Vol. 61. Р. 93–101.
4. Девятков Н. Д., Голант М. Б., Бецкий О. В. Миллиметровые волны и их роль в процессах жизнедеятельности. Москва: Радио и связь, 1991. 168 с.
5. Шкорбатов Ю. Г., Шахбазов В. Г. Биоэлектрические свойства клеточных ядер. Успехи совр. биол. 1992. Т. 112,
вып. 4. С. 499–510.
6. Способ исследования функционального состояния человека: пат. 2009494, Россия. C1 RU GO1 №33/483 / В. Г. Шахбазов, Ю. Г. Шкорбатов. Открытия. Изобретения. 1994. № 5.
7. Shckorbatov Y. G., Shakhbazov V. G., Navrotskaya V. V., Grabina V. A., Sirenko S. P., Fisun A. I., Gorobets N. N.,
Kiyko, V. I. Application of intracellular microelectrophoresis to analysis of the influence of the low-level microwave radiation on electrokinetic properties of nuclei in human epithelial cells. Electrophoresis. 2002. Vol. 23, N 13. Р. 2074–2079.
8. Сиренко С. П., Григорьева Н. Н., Шахбазов В. Г., Фисун А. И., Белоус О. И., Горобец Н. Н., Кийко В. И. Действие сантиметровых и миллиметровых электромагнитных волн линейной и круговой поляризации на клетки буккального эпителия человека. Материалы XI Междунар. Крымской конф. «СВЧ-техника и телекомуникационные технологии» (КрыМиКо’2001). 2001. С. 97–98.
9. Белоус О. И., Брюзгинова Н. В., Сиренко С. П., Фисун А. И. Контроль биологической эффективности действие электромагнитных полей миллиметрового диапазона. Радиофизика и электроника. 2015. Т. 6(20), № 4. С 98–102.
10. Шахбазов В. Г., Колупаева Т. В., Григорова И. А., Возницина К. Б. Изменение биологического возраста у больных с энцефалопатиями. Тезисы доклада, представленного на III Конгрессе геронтологов и гериатров Украины. 2000.
11. Мячина О. В., Зуйкова А. А., Пашков А. Н. Электрокинетическая активность клеток буккального эпителия у больных гипертонической болезнью. Сибирский медицинский журнал. 2012. Т. 27, № 2. C. 120–122.
12. Arkhypova K. A., Bilous O. I., Bryuzginova N. V., Fisun A. I., Malakhov V. O., Nosatov A. V., Sirenko S. P., Yemets B. G.
Role of mikrowave radiation in self-blood therapy.












Этот комментарий был удален автором.
ОтветитьУдалитьДобрый вечер, Сабухи. Я имею ваш тринити не изза рекламы сколько изза того что сам физик и был увлечен идеей биорезонанса. Когдато давно поступил в аспирантуру по биофизике в Москве, но бросил потому что нужно было заниматься еще и химией которую не любил. Я знаю эффективность метода. Режимы выбрать можно, но непонятно какая должна быть интенсивность этого низочастотного сигнала, т.к. динамика сигнала в разных тканях для разных органов разная. Кроме того, с точки зрения медицины хотелось бы понять эффективность, чувствительность, и возможные побочные эффеты.Я нигде не читал этого.
ОтветитьУдалить